Ce produit est si familier qu'il en apparaît banal et sans aucun mystère. Et pourtant ses multiples usages mettent en oeuvre des principes scientifiquesfondamentaux.
Pourquoi le sel est-il blanc?
En réalité, lorsque le sel est à
la fois très pur et parfaitement cristallisé,
il est totalement incolore! Un monocristal de sel est
transparent: on l'obtient par lente cristallisation
contrôlée. Les impuretés emprisonnées
dans les cristaux de sel, à commencer par l'humidité,
sont responsables de sa coloration blanche, par diffusion,
réfraction et réflexions multiples de
la lumière à l'intérieur des cristaux.
Certaines formes de sel ont d'autres couleurs, provenant
d'autres impuretés que l'eau. Par exemple, le
sel gris de Guérande, qu'affectionnent les gourmets,
est de teinte grisâtre, car il a cristallisé
en colonnes verticales à partir du fond du marais
salant, et il s'est donc contaminé de particules
de divers minéraux.
Comment les mines de sel se sont-elles formées?
Le sel peut s'obtenir par évaporation à
l'air libre de l'eau de mer dans des marais salants,
lorsque le climat le permet, c'est-à-dire lorsque
la belle saison ensoleillée n'est pas entrecoupée
de pluies qui viendraient détruire la récolte.
C'est l'une des plus belles utilisations de l'énergie
solaire. Certaines mers (Caspienne, Mer Morte, Grand
Lac Salé) ont de fortes salinités, car
l'évaporation l'emporte sur l'apport par les
rivières et fleuves des sels minéraux
lessivés des sols par les pluies. À l'extrême,
lorsqu'une mer a ainsi disparu, il ne reste plus à
sa place qu'une évaporite de sel. Lors des temps
géologiques, petit à petit, les couches
de sel d'évaporites marines (premier stade)
furent écrasées par des sédiments
plus denses (second stade). Aussi, on assiste ensuite
au cours des temps géologiques à une
remontée du sel par les fissures de l'écorce
terrestre, un peu comme de la crème venant surnager
sur du lait. Ce mouvement d'un minéral, un solide
dur et rigide pourtant, est un écoulement lent
du sel. Il s'effectue, à l'échelle microscopique,
par glissement des plans contenant les atomes, le long
des lignes de dislocation du cristal. Se forment ainsi
des colonnes de sel remontant des basses couches de
l'écorce terrestre. Ces colonnes de sel (ou
diapirs) se coiffent, près de la surface, de
chapiteaux en forme de dômes. Ce sont ces "chapeaux
de champignons" de sel qu'on exploite pour ce
minerai dans les mines de sel. Par exemple, on trouve
de tels gisements en Lorraine, en Pologne et au Texas.
On les exploite par des forages, suivis de l'injection
d'eau bouillante et du pompage de la saumure ainsi
produite.
Pourquoi la glace des poles est-elle de l'eau douce?
L'eau de mer est une solution saline. En moyenne, sa
salinité est de 35 g par litre.Lorsqu'on fait
s'évaporer un tel liquide, qui est un mélange,
on assiste d'abord au départ de la composante
la plus volatile. En l'occurrence, c'est l'eau. Vous pouvez vous en convaincre
facilement, par l'expérience suivante: goûtez
un peu du givre formé sur les parois internes
à votre réfrigérateur. Il n'a
aucun goût salé, il est fait d'une eau
en fait très pure, bien qu'il provienne des
fruits, légumes et autres denrées contenues
dans l'armoire frigorifique, toutes constituées
de mélanges aqueux. L'évaporation a fourni
un liquide pur, que le froid a condensé en cristaux
sur les parois. En cas de besoin, on peut faire fondre
ce givre et obtenir une eau distillée et déminéralisée,
par exemple pour en alimenter la solution acide de
l'accumulateur d'une voiture.De même, en montagne,
la neige et la glace sont aussi de l'eau pure, une
eau distillée trop pauvre en sels pour être
potable telle quelle. Or les précipitations
atmosphériques sur les sommets, qui les garnissent
de névés, glaciers et autres neiges éternelles,
viennent des nuages, c'est-à-dire de vapeur
d'eau pompée par la chaleur du soleil, aux océans
en majeure partie.Plus généralement,
lorsqu'un mélange tel que l'eau salée
s'évapore, ou cristallise, il fournit un corps
pur. C'est une méthode de purification très
efficace qu'on nomme, suivant le cas, distillation
ou cristallisation. Ainsi, la glace de la banquise
est-elle une eau très pure: elle résulte,
elle, d'une cristallisation. On a d'ailleurs proposé
de remorquer des icebergs, c'est-à-dire des
excroissances de glaciers, pour fournir en eau potable
des régions désertiques telles que le
Golfe Persique; mais de tels projets restent du domaine
de l'utopie.
Comment dessale-t-on l'eau de mer?
Puisque remorquer des icebergs n'est guère envisageable,
pour son coût, comme pour la sécurité
de la navigation, dessaler l'eau de mer est indispensable
pour fournir en eau de boisson une population, confinée
dans un lieu clos comme un sous-marin nucléaire,
ou vivant dans une région aride, comme l'Arabie
Saoudite ou la Sud Californie. L'un des procédés
de dessalement les plus utilisés à présent
consiste donc à chauffer l'eau de mer dans une
chaudière et à la distiller. Lorsque
la vapeur a été condensée, on
peut recueillir une eau très pure. Pour fixer
les idées, au départ d'eau de mer dont
la salinité, mesurée en ppm (parties
par million) est 35 000, l'eau douce de distillation
ne contient plus qu'une quantité infime, entre
1 et 50 ppm seulement de sel.Une variante est le procédé
de distillation à effet multiple: il tire parti
de ce que la vaporisation de l'eau se fait à
des températures largement inférieures
à 100oC sous un vide partiel. Un autre procédé
thermique de dessalement lui aussi, est la distillation
éclair. Si on chauffe de l'eau à 100oC,
et si on la maintient sous pression, avant de l'introduire
dans une enceinte où on a fait le vide, on assiste
à une transition très rapide, le liquide
se transforme en un éclair en vapeur. Ces deux
autres procédés thermiques, distillation
à effet multiple, et distillation éclair,
fournissent aussi une eau très pure (1-50 ppm
de sels). Il existe d'autres procédés
de dessalement.
Pourquoi le sel tue les limaces?
Saupoudrez du gros sel sur une limace: vous la retrouvez
morte, dans une petite flaque d'eau salée. Cet
animal est fait de cellules, dont chacune est un sac
microscopique, avec une solution aqueuse à l'intérieur.
Or, les parois de ces cellules, ou membranes, sont
perméables. Elles laissent passer l'eau. Lorsque
une membrane cellulaire sépare deux compartiments
aux teneurs en sel différentes, sa perméabilité
les fait communiquer: de l'eau migre de la solution
la moins salée vers la solution la plus salée.
Ainsi, la limace perd tant d'eau, lorsque ses cellules
l'expulsent pour s'efforcer de diluer le sel environnant,
qu'elle en meurt. C'est ce qui rend l'eau de mer modérément
toxique à la boisson: elle cause, paradoxalement,
une plus grande déshydratation encore. C'est
l'un des dangers pour les rescapés d'un naufrage
; le Dr. Alain Bombard, "naufragé volontaire"
prouva néanmoins la possibilité de survivre,
en ne buvant que de menues quantités d'eau de
mer.
Pourquoi le sel fait-il dégorger les concombres?
Pour la même raison qu'il extrait l'eau des limaces:
le concombre épluché et découpé
en rondelles, lorsqu'on les met au contact de sel,
l'avidité de celui-ci pour l'eau (imputable
à celle des cations sodium Na+ et anions chlorure
Cl- qui le composent) fait se dissoudre les cristaux
de sel dans l'eau issue des cellules du concombre.
Le processus de dégorgement (une déshydratation
donc) est accéléré au soleil et
à la chaleur.Plus généralement,
saler une denrée alimentaire permet d'en oter
une part de l'eau qu'elle contient. Le sel a de plus
un rôle désinfectant: il ne tue pas que
les limaces!
Quel est le rôle du sel dans les salaisons?
La toxicité du sel n'est pas restreinte aux organismes
pluricellulaires. Le sel, s'il est prodigué
en abondance, tue aussi la plupart des bactéries.
L'humanité en a tiré parti, depuis les
temps préhistoriques, pour protéger ainsi
de la corruption la viande excédentaire, qu'elle
veut conserver. Le sel permet ainsi, en complément
à ou à la place de la réfrigération
(elle aussi très ancienne), la conservation
de nombreux aliments. Encore de nos jours, on consomme
couramment de telles protéines animales ainsi
protégées à l'égard de
la prolifération de micro-organismes toxiques:
citons, entre autres, le jambon de montagne ou de Bayonne,
le saucisson (l'étymologie du mot reflète
d'ailleurs sa préparation), la morue salée
... Le caquage, c'est-à-dire la salaison du
hareng, découvert aux Pays-Bas au XIVe ou au
XVe siècle, aida l'expansion du commerce maritime
néerlandais; et permit les grands voyages de
découverte des XVIe-XIXe siècles. De
même, la salaison du poisson péché
permit les pèches au long-cours des pécheurs
européens, malouins entre autres, au large de
Terre-Neuve, à partir du XVIIe siècle.
Pourquoi saler l'eau de cuisson des aliments?
À l'inverse du dégorgement par le sel
de la limace ou du concombre, on veut éviter
d'assister à un engorgement des cellules de
l'aliment, animal ou végétal, placé
par omission dans une eau de cuisson non salée,
par l'eau faisant irruption à l'intérieur
de ces cellules. Faites cuire un oeuf dur dans de l'eau
douce, sa coquille éclatera, c'est probable.D'autre
part, l'eau salée bout à température
plus élevée que l'eau pure; le temps
de cuisson est donc diminué.
Pourquoi sale-t'on
une route enneigée?
L'eau salée a non seulement une température
d'ébullition plus élevée, mais
une température de fusion du solide (glace)
plus basse. Cela vient de ce ce que, si glace et vapeur
d'eau sont des corps purs, l'eau salée est un
mélange, donc désordonné et ce,
d'autant plus qu'on a mis davantage de sel.Ainsi, certains
mélanges réfrigérants (eau + sel
+ glace) ont-ils des températures de fusion
comprises entre - 15 et -20oC. Si vous souhaitez rafraîchir
plus rapidement votre champagne, salez le contenu de
votre seau à glace.C'est la même raison
qui fait épandre du sel sur les routes enneigées:
l'eau demeure liquide à température plus
basse, et la route reste donc exempte de verglas.
Pourquoi une carence en sel donne-t'elle des crampes
musculaires?
Revenons à la migration d'eau au travers des
membranes des cellules, d'une solution diluée
vers une solution concentrée. Elle se poursuit
jusqu'à l'équilibre, lorsque les concentrations
ont pu s'égaliser de part et d'autre de la membrane.
La concentration est la quantité de matière
(ici la quantité de sel dissous) par unité
de volume.

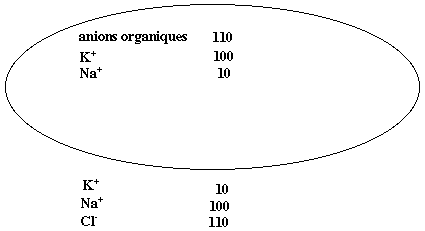
Figure 1: Comparaison des concentrations (en unités
mM) des principaux anions et cations à l'intérieur
et à l'extérieur d'une cellule-type.
On note l'électroneutralité dans chacun
de ces compartiments, puisque les totaux d'ions positifs
et négatifs sont égaux. On note aussi
l'entrée de potassium dans la cellule, et son
expulsion du sodium.
Ainsi, les cellules des organismes éjectent le
sodium Na+ et font entrer le potassium K+. De ce fait,
d'importantes différences de concentration existent
entre l'intérieur et l'extérieur d'une
cellule, d'un facteur 10 pour chacun de ces ions, comme
on le voit. Outre ces différentiels de concentration,
les cellules utilisent un moteur mu par l'énergie,
leur venant de l'hydrolyse de l'adénosine triphosphate
(ATP), pour pomper ces ions potassium et sodium, dans
un rapport de trois sodium pour deux potassium. La
conséquence est de doter la cellule de charges
électriques négatives sur son pourtour,
à l'intérieur de la membrane, et positives
à l'extérieur.C'est le cas des cellules
nerveuses, ou neurones: au repos, elles montrent un
potentiel électrique au niveau de l'axone le
tube reliant les deux extrémités d'un
neurone, avec les dendrites d'un côté
et les synapses de l'autre d'environ - 50 mV. Lorsque
le neurone est excité, le potentiel électrique
augmente très rapidement, passe par la valeur
zéro, grimpe jusqu'à + 50 mV environ,
puis revient à sa valeur de repos en fait,
en passant par un minimum plus bas encore, d'environ
- 60 mV. La montée vers le maximum, ou potentiel
d'action, provient de l'irruption d'ions sodium dans
l'axone; les concentrations initiales dans un rapport
10 justifient une variation de + 58 mV. Elle s'accompagne
de l'expulsion d'ions potassium, ce qui explique la
redescente vers un minimum, avant le retour à
la position de repos. Ces entrées et sorties
d'ions sont schématisées dans la Figure
2:
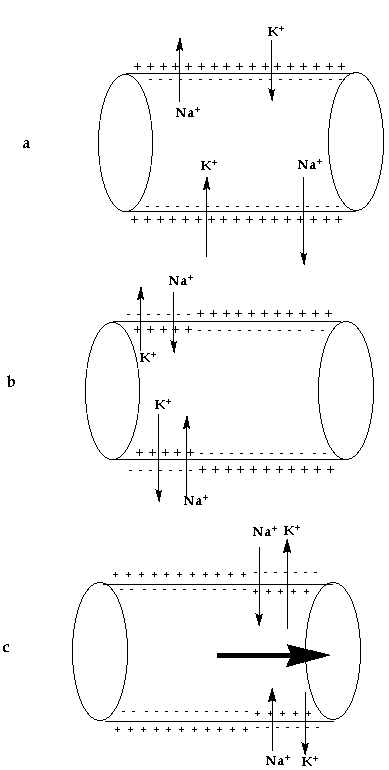
Figure 2: a: au repos l'axone d'un neurone est polarisé,
avec des charges négatives à l'intérieur
et des charges positives à l'extérieur
de la membrane; de ce fait, la différence de
potentiel membranaire est - 50 mV. b: l'entrée
de cations sodium et la sortie de cations potassium,
ou dépolarisation, font monter cette différence
de potentiel à + 40 mV avant de la faire revenir
à - 50 mV. c: le déplacement de cette
dépolarisation le long du neurone est l'influx
nerveux.
Le fonctionnement de notre système nerveux, représentatif
en cela de toutes les autres cellules du corps, exige
donc le maintien d'une quantité suffisante de
sel. C'est la raison pour laquelle nous ingérons
un à deux grammes de sel par jour. Une déficience
en sel, provenant en général d'une trop
grande excrétion (nous excrétons 90-95%
du sel ingéré, sous forme d'urine et
de sueur), se fait immédiatement sentir: en
particulier par des crampes musculaires nocturnes,
des mollets entre autres. C'est un signal d'alarme.
Il nous rappelle que le sel est indispensable à
la vie.
D'où vient le goût salé?
Chimiquement parlant, le sel est un composé;
c'est du chlorure de sodium. La saveur détectée
par les récepteurs du goût, sur la langue,
est celle des cations sodium Na+. Le bicarbonate de
sodium (ou, comme préfèrent dire les
chimistes, le carbonate acide de sodium), et d'autres
sels sodiques ont aussi une saveur salée.
Pourquoi l'industrie chimique a-t-elle besoin de sel?
Le sel est une importante matière première
pour l'industrie chimique. Elle en tire à la
fois le chlore et la soude: l'électrolyse d'une
saumure, c'est-à-dire d'une solution aqueuse
de sel, fournit la soude NaOH à l'une des électrodes
baignant dans la solution, et le chlore Cl2 à
l'autre électrode. C'est l'une des rares coproductions
de la chimie lourde: en effet, il est rare que les
périodes de forte demande économique
en chlore et en soude coïncident. Le chlore sert,
entre autres, à transformer l'éthylène
en chlorure de vinyle, qui est à son tour polymérisé
en polychlorure de vinyle ou PVC, qui est l'une des
matières plastiques les plus utilisées,
dans la construction en particulier.La soude a elle
aussi de nombreuses utilisations: par exemple, elle
sert à hydrolyser, c'est-à-dire à
couper en fragments plus petits, les polymères
naturels que sont la cellulose et la lignine des arbres
pour en faire de la pâte à papier.
Pierre Laszlo
Tous droits réservés à La Recherche, 1997.